双载药纳米药物载体系统用于肿瘤协同化疗已引起广泛的关注。然而,大多数双载药纳米药物系统在体内循环时间较短,显著降低了协同化疗药物的疗效和使用效率。长时间的血液循环能够确保纳米药物体系与病灶部位较长的接触时间,增强药物对肿瘤部位的靶向性和药物在肿瘤部位的浓度,从而提高疗效、减少毒副作用。目前提高纳米药物系统血液循环时间的方法主要包括纳米颗粒的表面改性、嵌段共聚物包封药物等。但是这些方法主要运用于单一药物化疗,载药量低和毒副作用大是其主要缺点,而双载药纳米药物系统长循环肿瘤协同化疗鲜有研究。而双载药纳米药物体系在血液中的循环时间决定了其治疗潜力,如何有效延长双载药纳米药物系统的血液循环时间仍是一个挑战,因此,利用新的策略构建高载药、低毒性且超长血液循环的双药纳米药物体系具有重要意义。
近日,西安交通大学生命学院生物医学影像与应用研究所吴道澄教授课题组从彩色条纹棒棒糖的结构得到启发,设计了一种新的策略构建了“棒棒糖结构”(lollipop-like)的超长血液循环双药纳米药物体系(图1)。他们首先将2种分子结构中具有大π键并有明显协同化疗作用的抗肿瘤药物阿霉素(DOX)和棉酚(Gossypol)通过π-π堆积组装形成纳米颗粒,由于阿霉素和棉酚水溶性不同和分子结构的差异,其π-π堆积不稳定并且其结合部分有大量空隙,加入小分子多巴胺将空隙填满,再逐渐聚合形成致密的聚多巴胺结构填补在药物分子之间将药物分子紧密的粘结在一起。这个现象就像砖缝(药物分子)之间灌满水泥(聚多巴胺)一样。具有极强粘附作用的聚多巴胺作为粘合剂牢固地填充在双药分子之间,不仅显著增强了纳米颗粒的稳定性,而且大幅度降低了药物释放的速度,达到了药物体内超长血液循环的目的。
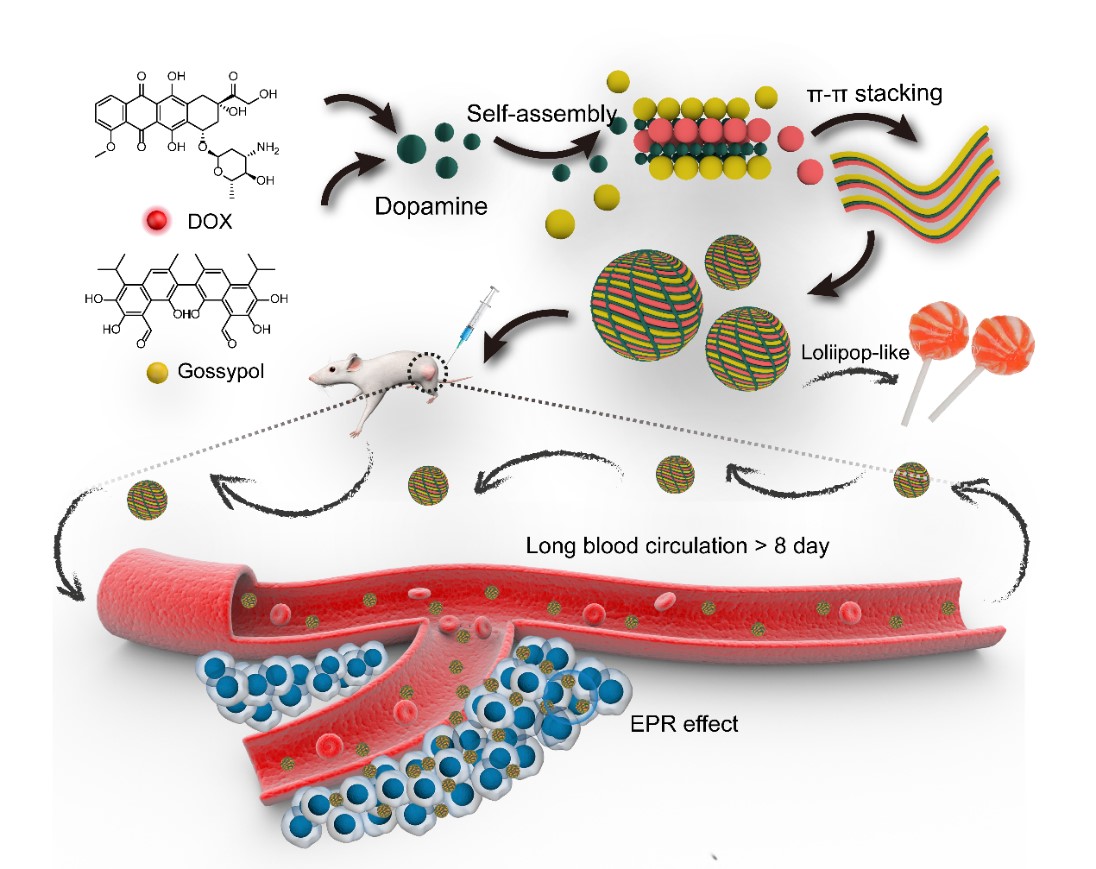
图1 “棒棒糖结构”的超长血液循环双药纳米药物体系
该双药纳米药物体系平均粒径59.6 ± 9.6 nm并具有明显的镶嵌结构、载药量高达91%。毒副作用很低,小鼠体内最大耐受剂量超过60 mg/kg,具有优良的双药治疗效果(协同指数0.23,指数越低协同治疗效果越好)。更为重要的是该体系有超长的体内血液循环时间(> 192 h,比游离药物增加258倍,消除半衰期增加458倍)。裸鼠注射8天以后在肿瘤部位药物蓄积量仍大于12%,用极低的药量可达到较高的抑瘤率(> 90%)。这种设计策略为未来双药纳米药物载体的发展提供了一种新的思路,为该双药纳米药物载体的临床应用打下了良好的基础。
该研究以“Ultra-long circulating lollipop-like nanoparticles assembled with gossypol, doxorubicin and poly-dopamine via π–π stacking for tumor synergistic therapy”为题在材料类国际权威期刊Advanced Functional Materials(影响因子13.325)上在线发表。西安交通大学生命学院生物医学信息工程教育部重点实验室为该论文的第一和通讯作者单位,生命学院博士研究生王雅为第一作者,吴道澄教授为通讯作者。该工作还得到了国家自然科学基金、国家重大仪器专项的支持。该研究是课题组继不同性质双载药纳米药物载体系统(Biomaterials 2015,39;131)、双药无限配位聚合物纳米系统(Biomaterials 2018,154;197)和光热-化疗一体纳米系统(Biomaterials 2018;88;12)肿瘤协同化疗研究以后的又一重要进展。
近年来,吴道澄教授课题组在双药纳米药物载体、磁性纳米材料和生物传感纳米载体方面取得了一系列研究进展,在国际权威期刊发表了一系列论文(包括Biomaterials 5篇;ACS Appl. Mater. Interfaces 3篇;J. Mater. Chem. A 1篇;Nanoscale 2篇等),这些研究成果具有重要的理论和实际意义。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.201805582
