术后粘连几乎是所有外科手术的后遗症之一。通常是指由伤口血栓、间皮损伤或异物(如纱布)引起的器官与周围组织之间的异常纤维化连接。术后粘连几乎可以发生在身体的任何部位,并可能导致多种风险(如肠梗阻、运动受限等)。因此,临床上对防粘连屏障的需求越来越大。理想的防粘连屏障应具有良好的粘弹性以满足具有不同运动模态的器官的生理活动需求(如动态收缩的心脏,蠕动的肠,准静态的肝脏等)。此外,屏障应具有不对称黏性(也被称作Janus性),以保证黏性面牢固附着于组织表面,而非黏性面与周围组织游离,从而起到防粘连效果。最后,屏障材料应该可以在内窥镜引导下经导管递送到组织表面,以满足日益增长的微创手术需求。然而,尚没有合适的防粘连屏障可以同时兼顾材料粘弹性、Janus组织黏附性与微创递送。
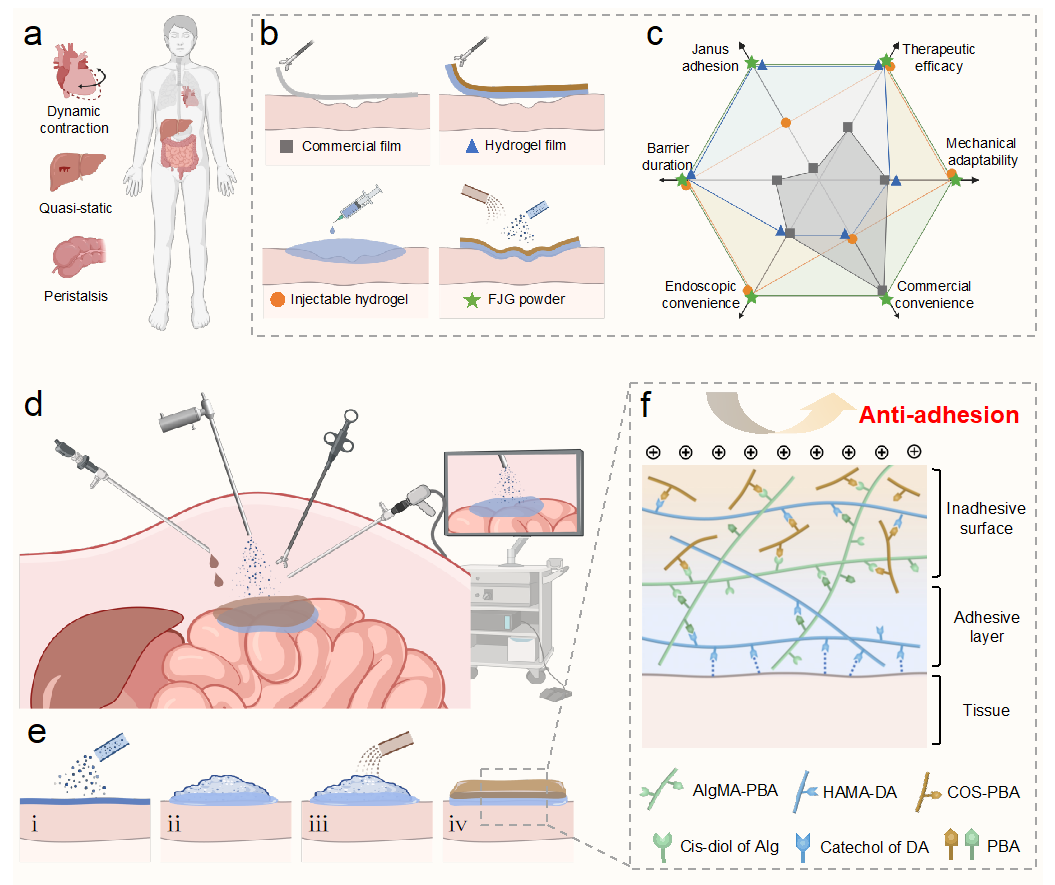
图1:FJG粉末设计和内镜递送示意图
针对上述问题,西安交通大学生命科学院与技术学院仿生工程与生物力学研究所(BEBC)依托交大“大医科+强工科”模式,充分利用交大多学科交叉和理工医融合的优势,与西安交通大学吕毅教授团队合作,在“外科梦工厂”的平台支持下,基于力学、材料学、外科学等多学科交叉,开发了一种快速凝胶化的粉末(FJG粉末),可以在内窥镜引导下通过导管递送,并在组织表面原位形成粘弹性Janus水凝胶屏障。粘弹性的FJG水凝胶可以防止多种器官(心、肝、肠)的术后粘连,并在临床前转化的大动物实验中验证了其在微创手术中的可行性及有效性。
该工作构建了一种可以快速吸水并凝胶化的水凝胶前体粉末,使用分层水合的策略,实现了在组织原位形成Janus水凝胶层。首先利用甲基丙烯酰化修饰破坏了大分子多糖的分子间作用,从而提高了大分子多糖的吸水能力;同时利用硼酸酯键的快速动态加成,使粉末在水合后快速凝胶化。在递送到组织表面后,FJG粉末会快速吸收组织表面水分并形成牢固黏附的水凝胶。进一步地,利用阳离子壳寡糖溶液将上层粉末水合并使上层水凝胶表面阳离子化,以获得上表面不具有黏性的Janus水凝胶。所形成的粘弹性FJG水凝胶可以适应于不同的器官运动,并具有适当的在体降解速率,可以有效地预防大鼠心脏、肝脏、肠等多器官的术后粘连。此外,为了推动FJG粉末的临床转化,开发了气体辅助的粉末递送装置,该装置可以在内窥镜辅助下,将FJG粉末均匀地递送到目标组织表面。同时,在临床前猪的肝脏粘连模型,进一步证明了FJG水凝胶预防术后粘连的效果。

图2:FJG粉末在内窥镜辅助下的微创手术中递送的标准流程示意图及临床前猪的手术演示图像
该工作以“可用于内镜手术下的快速成胶的双面粉末用于防止术后黏连”( An endoscopically compatible fast-gelation powder forms Janus-adhesive hydrogel barrier to prevent post-operative adhesions)为题,在国际期刊《美国科学院院报》(PNAS)上在线发表。西安交通大学生物医学信息工程教育部重点实验室为该论文的第一作者单位和通讯作者单位。这是该团队两个月内的发表的第二篇PNAS论文。文章第一作者为西安交通大学生命学院博士生贾渊博,通讯作者为西安交通大学生命学院徐峰教授、西安交通大学第一附属医院吕毅教授和魏钊副教授。文章其他作者包括博士生冯锦腾、冯哲、刘婧仪、杨燕申、雷萌、第四军医大学唐都医院骨科李小康副教授和西安交通大学第一附属医院郭卉教授。
该工作得到了国家自然科学基金、西安交通大学青年人才支持计划和中央高校基本科研业务费资助项目的资助。
西安交通大学仿生工程与生物力学研究所(BEBC)围绕“科学研究-技术研发-工程应用-临床推广”的学术思想和“临床问题(BED)-实验室研究(BENCH)-临床应用(BED)”的研究思路,在力学微环境领域开展了从组织到细胞和分子尺度的多尺度生物热-力-电耦合学等基础和应用研究,为阐明重大疾病的发病机理和临床诊疗提供有效的理论指导和技术方案。特别是近年来,在力学生物学的研究基础上,通过工程学手段,将不同尺度的力学调控引入疾病治疗,开展了一系列的“力医学(mechanomedicine)”研究,相关代表性研究成果发表于Nature Materials (2017,2022)、Nature Chemistry (2019)、Nature Biomedical Engineering (2021,2020)、PNAS (2022)、 Nature Communications (2022,2021)、Science Advances (2019)等期刊。
论文链接:https://www.pnas.org/doi/10.1073/pnas.2219024120
BEBC网站主页:http://bebc.xjtu.edu.cn/
